Niedoczynność tarczycy (hipotyreoza) jest zespołem chorobowym wynikającym z niedoboru hormonów tarczycy poniżej poziomu pokrywającego aktualne potrzeby organizmu lub też z powodu oporności obwodowej tkanek na działanie hormonów tarczycy. Objawy kliniczne zależą od stopnia niedoboru hormonów tarczycy oraz okresu życia, w którym choroba się ujawniła.
Wrodzoną niedoczynność tarczycy (WNT) rozpoznaje się, jeżeli dysfunkcja układu podwzgórze - przysadka - tarczyca występuje od okresu życia płodowego. WNT może mieć charakter trwały, gdy utrzymuje się przez okres całego życia chorego lub przejściowy, kiedy niedoczynność tarczycy występuje w pierwszych miesiącach życia, a po ustaniu działania czynników wywołujących stan hipotyreozy funkcja tarczycy normalizuje się.
Częstość występowania WNT w krajach europejskich ocenia się na 1 : 3000 do 1 : 4000 urodzeń żywych. Częstość WNT w różnych krajach przedstawia się następująco: Estonia 1 : 2860, Holandia 1: 3000, Walia 1 : 3279, Szwajcaria 1 : 3300, Francja 1 :3500, Austria 1 : 3650, Szkocja 1 : 4400. W Polsce w 1998 r częstość WNT wynosiła 1 : 3810. Biorąc pod uwagę chorobowość z ostatnich lat można szacować, że w Polsce rocznie rodzi się 100 - 120 noworodków chorych na WNT.
Przyczyny
Przyczyny wrodzonej niedoczynności tarczycy mogą być różne. Najczęstsze z nich to:
- dysgenezja tarczycy
- Dysgenezja czyli wady rozwojowe gruczołu tarczowego są przyczyną 70-80% przypadków trwałej hipotyreozy. Do grupy zaburzeń rozwojowych należy agenezja (atyreoza) tj. brak tkanki tarczycowej w organiźmie, hipoplazja (niedorozwój) tarczycy oraz ektopia tzn. nieprawidłowe położenie tkanki tarczycowej np. na podstawie języka, w okolicy podbródkowej , nad- podgnykowej, wewnątrzkrtaniowo, w obrębie przetrwałego przewodu językowo - tarczowego lub rzadziej zamostkowo czy w jamie brzusznej. Dysgenezja tarczycy częściej dotyczy dziewczynek. Stosunek dziewcząt do chłopców określa się na 2 : 1. Opisuje się też rzadkie przypadki rodzinnego występowania dysgenezji tarczycy.
- dyshormonogeneza
- Dyshormonogeneza stanowi 15-30% przyczyn trwałej hipotyreozy. Terminem tym określamy wrodzone zaburzenia biosyntezy hormonów tarczycy, dziedziczone najczęściej jako cecha autosomalna recesywna, rzadziej dominująca. Wymienia się sześć typów genetycznie uwarunkowanych defektów syntezy hormonów tarczycy. Zaburzenie jakiegokolwiek etapu biosyntezy prowadzi do zmniejszenia produkcji T4 i T3, co powoduje wzrost wydzielania TSH przez przysadkę, a w efekcie rozwój wola. Objawy dyshormonogenezy zależą od głębokości defektu. Najcięższe postacie prowadzą do hipotyreozy utrzymującej się od okresu płodowego, defekty łagodniejsze manifestują się obecnością wola ze skompensowaną funkcją tarczycy.
- oporność tkanek obwodowych na hormony tarczycy
- Zespoły oporności tkanek na działanie hormonów tarczycy są rzadko występującymi zaburzeniami zależnymi od uszkodzenia lub braku receptorów T3 w komórkach. Oporność może mieć charakter uogólniony, może dotyczyć wyłącznie przysadki mózgowej, albo też dotyczy tkanek obwodowych z wyłączeniem przysadki - stąd wynika różnorodność obrazu klinicznego i odchylenia w badaniach hormonalnych. Dziedziczy się w sposób autosomalny recesywny lub dominujący - wówczas występuje rodzinnie.
- niedoczynność tarczycy podwzgórzowo-przysadkowa
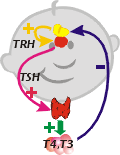
- Wrodzona niedoczynność tarczycy podwzgórzowo - przysadkowa występuje znacznie rzadziej niż niedoczynność pierwotna, a jej przebieg kliniczny jest łagodniejszy. Wrodzone nieprawidłowości podwzgórza i/lub przysadki mózgowej mogą wynikać z obecności wad rozwojowych lub uszkodzenia tych struktur w wyniku niedotlenienia, infekcji, procesów autouimmunologicznych w okresie życia płodowego, co prowadzi do deficytu TRH lub TSH, Najczęściej ujawnia się wówczas wielohormonalna niedoczynność przysadki.
- przejściowa niedoczynność tarczycy
- Wśród przyczyn przejściowej niedoczynności tarczycy
najczęściej wymienia się niedobór lub nadmierną podaż jodu w okresie
ciąży. Dla prawidłowej czynności tarczycy płodowej konieczna jest
odpowiednia zawartość jodu w diecie matki oraz jego transport
przezłożyskowy. Wiadomo, że na obszarach nasilonego niedoboru jodu
częściej występuje niedoczynność tarczycy oraz wole noworodkowe.
Badania populacji polskiej z początku lat 90 potwierdziły występowanie
na niektórych obszarach centralnej i południowo-wschodniej Polski
umiarkowanego niedoboru jodu. Od 1996r prowadzona jest profilaktyka
jodowa poprzez obligatoryjne jodowanie soli kuchennej. Zapotrzebowanie
kobiety ciężarnej na jod określono na 200 ug / dobę. Z drugiej strony
wiadomo, że tarczyca płodu nie ma wykształconych mechanizmów
chroniących przed nadmiarem jodu, dlatego duża jego podaż prowadzić
może do zahamowania syntezy hormonów tarczycy. Nadmiar jodu wynikać
może ze stosowania u ciężarnej leków zawierających jod (np. jodek
potasu wykrztuśnie), jodowych środków kontrastowych lub odkażających.
Jod radioaktywny 131 podany matce niszczy tarczycę płodu.
W chorobach autoimmunologicznych tarczycy u matki obecne przeciwciała przenikają przez łożysko. Przeciwciała blokujące receptor TSH, a prawdopodobnie i przeciwtarczycowe hamują syntezę hormonów tarczycy u płodu. Efekt hamujący wywierają również tyreostatyki przyjmowane przez kobietę w ciąży. Bierze się także pod uwagę możliwość ograniczenia syntezy hormonów tarczycy u płodu, gdy matka przyjmuje inne leki np. sulfonamidy, preparaty kobaltu.
Objawy
Objawy WNT u noworodka nie są charakterystyczne i mogą być dyskretnie wyrażone. W wywiadzie dotyczącym przebiegu ciąży i porodu w niektórych przypadkach stwierdza się ciążę przenoszoną do 42 Hbd, słabe ruchy płodu, leniwą akcję porodową, wielowodzie. Noworodek rodzi się zwykle z prawidłową masą i długością ciała. W ciągu pierwszych tygodni życia stopniowo ujawniają się cechy hipotyreozy. U około 1/3 chorych dominującym objawem jest przedłużona żółtaczka noworodków, sucha marmurkowa skóra, obecność przepukliny pępkowej, mniejsza ruchliwość, niechęć do ssania, zaparcia. Dzieci są spokojne, dużo śpią, mało płaczą, głos jest niski, ochrypły. W pierwszym miesiącu życia uwidacznia się powiększenie języka, co może być przyczyną zaburzeń oddychania. Obserwuje się obniżenie napięcia mięśniowego, brzuch jest duży, rozlany, mogą występować obrzęki, zwłaszcza na twarzy. Wczesnymi objawami hipotyreozy wskazującymi na niedobór hormonów u płodu są zmiany w układzie kostnym: opóźnione dojrzewanie kości widoczne w badaniach radiologicznych (u noworodka brak jąder kostnienia w nasadzie dalszej kości udowej i nasadzie bliższej kości piszczelowej). niezarośnięte szerokie szwy czaszkowe, otwarte tylne ciemiączko.
Objawy uszkodzenia centralnego układu nerwowego zależą od stopnia niedoboru hormonów tarczycy u płodu oraz pourodzeniowego czasu trwania hipotyreozy. O przebiegu rozwoju psychoruchowego dziecka decyduje wczesne wprowadzenie leczenia substytucyjnego. W ciężkich przypadkach, zwłaszcza późno rozpoznanych ujawnia się upośledzenie umysłowe różnego stopnia. W okresie niemowlęcym widoczne jest opóźnienie rozwoju psychomotorycznego, dzieci są spowolniałe, późno zaczynają siadać i chodzić. Dzieci starsze wykazują obniżoną sprawność intelektualną, występują zaburzenia mowy. Częstym objawem hipotyreozy wrodzonej jest uszkodzenie móżdżku, w postaci drżenia zamiarowego, niezborności ruchów aż do obrazu ataksji móżdżkowej. Stwierdzono, że nawet pomimo wczesnego wprowadzenia właściwego leczenia u niektórych dzieci utrzymują się cechy specyficznych zaburzeń w rozwoju mózgu, których wyrazem są zaburzenia równowagi, niezręczność, trudności w uczeniu się, zaburzenia zachowania.
Leczenie
Leczenie substytucyjne WNT polega na doustnej podaży soli sodowej L-tyroksyny. Celem leczenia jest uzyskanie przez dziecko chore prawidłowych wskaźników rozwoju somatycznego i psychicznego, co wiąże się z wczesnym wprowadzeniem terapii oraz stosowaniem odpowiednich dawek l-tyroksyny. Obecnie postuluje się wdrożenie leczenia substytucyjnego w drugim tygodniu życia. Wielkość dawki inicjującej leczenie noworodka ciągle jest przedmiotem dyskusji.
Monitorowanie leczenia polega na ocenie rozwoju fizycznego i kontroli badań hormonalnych w surowicy (FT4, TSH, ewentualnie T4) co 3 miesiące u niemowląt i dzieci do 2 lat oraz co 6 miesięcy u dzieci starszych. Przy dobrze prowadzonej substytucji dziecko wykazuje prawidłowe tempo wzrastania, a poziom T4 i FT4 w surowicy utrzymuje się w górnym zakresie normy dla wieku. Raz w roku wskazane jest badanie wieku kostnego dla oceny rozwoju somatycznego.