Wstęp
Badania przesiewowe noworodków mają na celu wczesne (przedkliniczne) wykrycie choroby wrodzonej u dziecka, tak aby przez wdrożenie leczenia zapobiec powstawaniu następowych wad rozwojowych, a zwłaszcza ciężkiego upośledzenia umysłowego.
Efektywność badań przesiewowych jako całego systemu organizacyjnego i diagnostycznego należy oceniać z punktu widzenia wypełniania celu klinicznego, kosztów ogólnie pojętych, w tym kosztów tzw. społecznych i ekonomicznych, oraz stopnia ryzyka popełnienia błędów diagnostycznych zarówno przez diagnozę fałszywie ujemną jak i fałszywie dodatnią.
Wprowadzony w całej Polsce system oceniany musi być według następujących podstawowych kryteriów dla badań przesiewowych:
- Powszechność
- Oczekuje się, że wszystkie noworodki objęte będą badaniem przesiewowym
- Czułość testu
- Jest to zdolność metody do wykrycia wszystkich dzieci z daną chorobą. Określa się ją jako stosunek liczby dzieci chorych wykrytych w badaniu przesiewowym do liczby dzieci chorych w całej populacji. Test idealny daje 100% czułości - czyli wszystkie chore dzieci zostały wykryte w badaniach przesiewowych. Czułość testu określa równocześnie ryzyko „zgubienia” dziecka chorego w badaniu przesiewowym.
- Selektywność testu
- Jest to zdolność metody do wykrywania jedynie dzieci chorych w badanej populacji. Określa sie ją jako stosunek liczby chorych w populacji do liczby wyników dodatnich w teście przesiewowym. Idealny test daje 100% gdy nie wykazuje wyników fałszywie dodatnich czyli choroba jest potwierdzona u każdego dziecka wezwanego do dodatkowej diagnostyki. Selektywność testu jest wskaźnikiem kosztów dodatkowych związanych z diagnostyką potwierdzającą, która wymaga badania klinicznego i laboratoryjnego, a także obciąża finansowo i psychicznie rodziców dziecka, którzy muszą przyjechać z 2-4 tygodniowym dzieckiem do odpowiedniej poradni lub kliniki.
- Użyteczność kliniczna
- Badanie przesiewowe jest użyteczne klinicznie jeśli wynik testu uzyskany jest w pierwszych tygodniach życia, tak aby rozpoczęte leczenie zapewniało ochronę przed wadami następowymi choroby wrodzonej. Obecnie rekomenduje się jak najwcześniejsze (w ciągu dwóch tygodni życia) zdiagnozowanie i leczenie hipotyreozy i fenyloketonurii. Konieczne jest rozpoczynanie leczenia w pierwszym miesiącu życia.
- Ekonomiczność
- Ekonomiczność badań przesiewowych obejmuje relatywną analizę kosztów oraz tzw. kosztów społecznych.
Kryteria doboru testów w badaniach przesiewowych
Zakład Badań Przesiewowych i Diagnostyki Metabolicznej w ramach prowadzonych badań przesiewowych zajmuje się również oceną przydatności testów diagnostycznych do masowych badań przesiewowych
Testy analityczne, a zwłaszcza testy do oznaczeń hormonalnych, pochodzące od różnych producentów różnią się między sobą - mimo iż służą do oznaczania tego samego czynnika. Testy te nie mogą być stosowane zamiennie gdyż odczyt wartośsci stężenia dla tej samej próbki krwi będzie różny zależnie od użytego zestawu. Dlatego praktycznie nie istnieje jednolity system norm dla poziomów hormonów we krwi i każdy z producentów zastrzega, że użytkownicy testu powinni ustalić własne normy, zwłaszcza że różnice odczytu mogą przekraczać 50%.
Z punktu widzenia masowych badań przesiewowych poza odczytem wartości bezwzględnej, czyli tzw. dokładnością testu, istotna jest jego precyzja, czyli zmienność wewnątrztestowa, międzytestowa i międzyseryjna, która decyduje w znacznym stopniu o ilości błędów fałszywie dodatnich i fałszywie ujemnych w badaniu przesiewowym.
Aby ocenić jakość określonego zestawu i przydatność do masowych badań przesiewowych należy wykonać ocenę jakości analitycznej zestawu oraz ocenę kliniczną na podstawie statystycznie wiarygodnej próby, z uwzględnieniem powtarzalności wyników w czasie, czyli porównywalności wyników uzyskanych np. w styczniu i sierpniu, z różnych partii produkcji. Jest to typowa procedura oceny testów stosowana przez odpowiedzialne ośrodki przesiewowe w świecie.
Stosowanie tych samych odczynników we wszystkich ośrodkach przesiewowych ma znaczenie nie tylko ekonomiczne ale również ważne znaczenie kliniczne, ponieważ pozwala na ocenę niektórych zjawisk w całej populacji noworodków w Polsce, np. prowadzonej od kilku lat oceny niedoboru jodu na podstawie poziomow TSH u noworodków.
Wdrożony przez Zakład i stosowany obecnie w całej Polsce system badań przesiewowych oparty jest o etykiety z kodem paskowym umożliwiającym komputerowy nadzór nad wszystkimi etapami badań. System ten zapewnia objęcie badaniami praktycznie wszystkich noworodków oraz zapewnia wyeliminowanie błędów technicznych w trakcie wykonywania badań. Bardzo ważnym czynnikiem jest więc zgodność testu z tym systemem lub możliwośc łatwej adaptacji testu do wymogów systemu.
Wybór testu dokonywany jest w drodze publicznego przetargu organizowanego przez Zakład Zamówień Publicznych w Misterstwie Zdrowia.
Oznaczanie stężenia tyreotropiny we krwi



Oznaczanie poziomu tyreotropiny (TSH - Thyroid Stimulating Hormone) stosowane jest do wykrywania hipotyreozy (wrodzonej niedoczynnośći tarczycy). Obecnie w całej Polsce stosowany jest test immunoluminetryczny
Wynik testu jest klasyfikowany na trzy grupy zależnie od poziomu TSH:
- norma
- podwyższony (wysyłka drugiej bibuły do rodziców)
- natychmiastowe wezwanie do lekarza
- Czułość testu
- W ostatnich czterech latach liczba dzieci wykrytych testem przesiewowym utrzymuje się na stałym poziomie, z potwierdzoną częstością tej choroby około 1 na 4000 żywo urodzonych noworodków Nie odnotowaliśmy ani jednego przypadku wyniku fałszywie ujemnego (dziecko chore ale nie wykryte w badaniach). Czułość testu jest zatem zbliżona do 100% - ponieważ według danych literaturowych w badaniach gubiono w różnych krajach ok. 2 - 3% dzieci chorych, co w polskiej populacji odpowiada 2 - 3 dzieci rocznie. Biorąc pod uwagę wyniki nasze oraz innych krajów, czułość całego systemu badań przesiewowych należy uznać za bardzo dobrą.
- Selektywność testu
- Selektywność testu w roku 1999 wyniosła 77% (121 dzieci leczone / 158 dzieci wezwane do diagnozy = 77%), co oznacza wzywanie średnio 1.3 dziecka na 1 dziecko chore. Jest to bardzo wysokie prawdopodobieństwo potwierdzenia hipotyreozy i zgłoszenie się rodziców z dzieckiem musi być szybko wyegzekwowane. Gdyby zrezygnować z wysyłania drugiej bibuły (wyniki z tzw. szarej strefy) to selektywnośc testu wyniosła by 16.5% - czyli na jedno dziecko chore przypadało by 6 dzieci wzywanych. Potwierdza to zasadność wysyłania drugich bibuł zamiast natychmiastowego wzywania dzieci do specjalistycznej przychodni.
Oznaczanie stężenia fenyloalaniny we krwi
Oznaczanie poziomu fenyloalaniny (Phenylalanine - Phe) stosowane jest do wykrywania fenyloketonurii.
Do roku 1997 w całej Polsce do oznaczania poziomu fenyloalaniny we krwi stosowany był test Guthrie. Jest to test mikrobiologiczny polegający na wzrokowej ocenie wielkości wzrostu bakterii wokół krążka z próbką krwi noworodka ułożonego na specjalnym podłożu. Test ten dzięki swej prostocie był powszechnie stosowany w całym świecie. Test ten ma jednak szereg wad:
- odczyt polega na wzrokowym porównaniu wielkości wzrostu bakterii wokół próbki badanej z wielkością wzrostu wokół próbki wzorcowej (próbki o znanym poziomie fenyloalaniny). Taki sposób odczytu jest odczytem nieobiektywnym tzn. ta sama próbka może być różnie oceniona przed różne osoby odczytujące. Powoduje to możliwość błędnego odczytu poziomu i zgubienia chorego dziecka
- Prawdopodobieństwo popełnienia błędu rośnie wraz z ilością czytanych prób czyli wraz z narastającym zmęczeniem osoby czytającej
- Próbki krwi (krążki bibuły o średnicy 5 mm) układane są na płytkach ręcznie co może powodować pomyłki przy identyfikacji danych dziecka od którego pobrano daną próbkę
- Wzrost bakteri nie występuje gdy próbka krwi zawiera antybiotyki którymi leczone było dziecko przed pobraniem próbki
- Odczyt poziomu fenyloalaniny wykonywany był kilka dni od otrzymania próbki - tak długi czas wynikał z konieczności dodatkowego przygotowania próbki krwi.
W roku 1997 w Pracowni rozpoczęto masowe oznaczanie fenyloalaniny za pomocą testu ilościowego kolorymetrycznego. Testy ilościowe wykonywane na czytnikach mikropłytek pozwalają na automatyzację oraz, co ważne, na kontrolę komputerową z zastosowaniem etykiet z kodem paskowym. Pozwoliło to również na ujednolicenie procedur badań dla testu w kierunku fenyloketonurii i hipotyreozy. Znacznie skrócony został czas po którym uzyskuje sie wynik - wynik może być uzyskany w tym samym dniu (lub w następnym) w którym próbka krwi dociera do laboratorium. Obecnie w całej Polsce stosowany jest test ilościowy (kolorymetryczny) firmy IBL.
Wynik testu jest klasyfikowany na trzy grupy zależnie od poziomu fenyloalaniny:
- norma
- podwyższony (wysyłka drugiej bibuły do rodziców)
- natychmiastowe wezwanie do lekarza
- Czułość testu
- Wstępna ocena czułości testu dokonana na podstawie
badania przesiewowego ponad 300.000 noworodków w latach 1997-1998
pozwala na bardzo wysoką ocenę czułości testu sięgającą 100%.
Uzyskana częstość fenyloketonurii na poziomie średnio 1:7000 żywo
urodzonych jest zgodna z wartościami uzyskiwanymi testem Gutrie. Nie
zgłoszono również przypadku wyniku fałszywie ujemnego (dziecko chore
lecz nie wykryte w badaniu).
Tak wysoka czułość testu kolorymetrycznego pozwoliła na zlikwidowanie dodatkowego pobierania próbek moczu od dzieci w wieku 3-4 tygodni. Próbka ta służyła do oznaczania obecności kwasu pirogronowego w moczu pojawiającego się w przypadku wysokiego poziomu fenyloalaniny we krwi. Oznaczanie kwasu pirogronowego w moczu wynikało z niskiej czułości testu Guthriego, dodatkowo skutecznośc pobierania próbek moczu była niska.
- Selektywność testu
- Selektywność testu w roku 1999 wyniosła 75% (56 dzieci z potwierdzoną fenyloketonurią / 75 dzieci wezwane do diagnozy = 75%), co oznacza wzywanie średnio 1.33 dziecka na 1 dziecko chore. Podobnie jak dla hipotyreozy jest to bardzo wysokie prawdopodobieństwo potwierdzenia fenyloketonurii i zgłoszenie się rodziców z dzieckiem musi być szybko wyegzekwowane.
Od roku 2017 test kolorymetryczny, w badanich przesiewowych noworodków, zastąpiony został badaniem metodą tandemowej spektrometrii mas.
Nowa metoda pozwala na równoczesne oznaczenie m.in. stężenia fenyloalaniny (Phe) i stężenia tyrozyny (Tyr) i obliczenia stosunku tych stężeń. Wykorzystanie
wartości stężenia fenyloalaniny i wartości stosunku Phe/Tyr pozwala na zwiększenie selektywności metody praktycznie do około 95%.
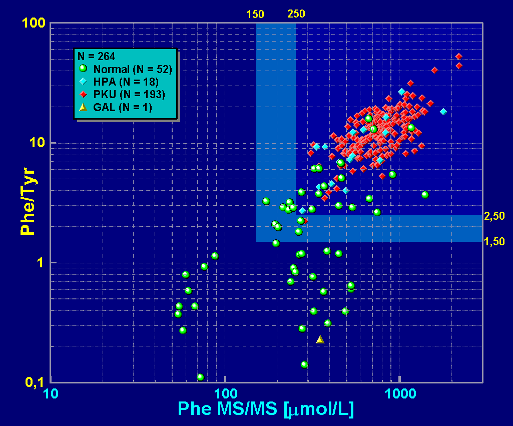
Skuteczność równoczenego zastosowania stężenia Phe i stosunku Phe/Tyr obrazuje poniższy wykres pokazujący zależność tych wartości dla bibuł
dla których podejrzewano PKU:
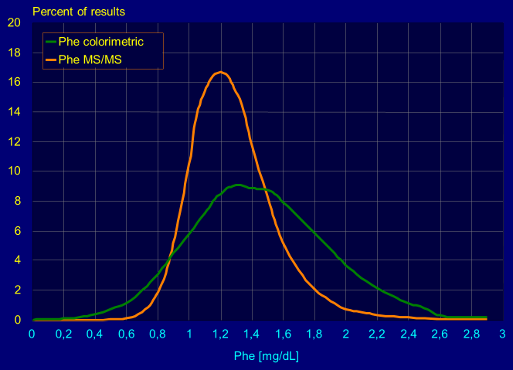
 Przykładowy wykres obrazujący większą dokładność testu metodą tandemowej spektrometri mas przedstawiony jest poniżej - wykres pokazuje dystrybucję
wyników oznaczanych dwoma metodami: kolorymetryczną (Phe colorimetric) i metodą tandemowej spektrometri mas (Phe MS/MS):
Przykładowy wykres obrazujący większą dokładność testu metodą tandemowej spektrometri mas przedstawiony jest poniżej - wykres pokazuje dystrybucję
wyników oznaczanych dwoma metodami: kolorymetryczną (Phe colorimetric) i metodą tandemowej spektrometri mas (Phe MS/MS):
Badanie IRT/DNA
Strategia obecnych badań przesiewowych w kierunku mukowiscydozy (CF) opiera się na oznaczeniu immunoreaktywnej trypsyny (IRT) we krwi na bibule i analizie DNA, polegającej na identyfikacji mutacji w genie CFTR (Cystic Fibrosis Transmembrane Conductance Regulator).
Jako pierwsze wykonywane jest oznaczenie IRT (IRT1) ilościową metodą ELISA z wysuszonych kropli krwi pobranych pomiędzy 3 a 6 dobą życia (w szpitalu krew jest pobierana na jedną wspólną dla hipotyreozy, fenyloketonurii i mukowiscydozy bibułę). W przypadku stężenia IRT1 powyżej normy tj powyżej 99,4 centyla, wykonywana jest - po uzyskaniu pisemnej zgody rodziców - analiza DNA
Analiza molekularna DNA wykonywana jest z wysuszonej kropli krwi z bibuły. Obecnie przyjęta strategia diagnostyczna, oparta w większości na sekwencjonowaniu, umożliwia identyfikację 675 znanych mutacji w badanym genie, z czego 15 należy do panelu mutacji najczęściej występujących w populacji polskiej.
Na badanie konsultacyjne wzywane są dzieci z zidentyfikowaną mutacją w jednym lub w obu allelach genu CFTR.
Konsultacja w ośrodku specjalistycznym.
Po udzieleniu rodzicom wstępnych informacji o wskazaniach do przeprowadzenia badań weryfikacyjnych, u wezwanych niemowląt wykonywane są testy potowe dwoma metodami: jontoforezą pilokarpinową (j.p.) wg Gibsona i Cooka oraz test konduktometryczny (t.k.) Wescor lub Nanoduct, którego wynik w przeciwieństwie do j.p. otrzymujemy bezpośrednio po wykonaniu badania.
Wykonywane są pomiary antropometryczne wysokości i masy ciała. Oceniany jest stanu zdrowia niemowlęcia, z uwzględnieniem objawów charakterystycznych dla CF. Rodzicom pacjenta udzielana jest informacja o wynikach analizy molekularnej, testu konduktometrycznego i dalszym postępowaniu diagnostycznym oraz wstępna porada genetyczna.

